8 år ago
Sulfat er en almindelig anion i vandmiljøet og spiller en vigtig rolle i biogeokemiske kredsløb. Det findes overalt, men dets forurening er blevet et stigende problem i de seneste år, især med accelerationen af industrialisering og urbanisering. En stigende koncentration af sulfat i vandet truer ikke kun menneskers sundhed og den økologiske balance, men kan også påvirke processer som karbonatforvitring og den globale kulstofcyklus.

Tidligere studier har vist, at når menneskekroppen indtager for meget sulfat, kan det føre til flere sygdomme, herunder diarré, dehydrering og mave-tarm-forstyrrelser. I vandmiljøet kan sulfat omdannes til giftige stoffer under visse forhold, hvilket resulterer i tab af essentielle metal-elementer i vandplanter og ændringer i den oprindelige øko-hydrologiske funktion. Studier har vist, at høje koncentrationer af sulfat kan forårsage død af ferskvandsinvertebrater. Verdenssundhedsorganisationen (WHO) og Kina begrænser sulfatkoncentrationen i drikkevand til mindre end 250 mg/L.
At identificere kilderne til sulfatforurening nøjagtigt er afgørende for at kontrollere problemet i vandmiljøet. Opløst sulfat i vandmiljøet stammer primært fra både naturlige og menneskeskabte kilder.
Kilder til Sulfat i Vandmiljøet
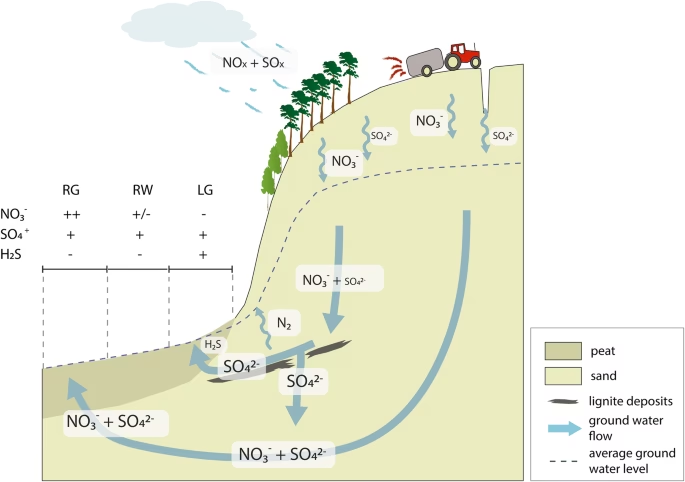
Naturlige kilder inkluderer opløsning af sulfatmineraler (f.eks. gips), oxidation af sulfidmineraler (f.eks. pyrit), nedbør og vulkansk aktivitet.
Menneskeskabte kilder omfatter spildevandsinfiltration, gødning, syntetiske rengøringsmidler, industrielt spildevand og minedrift. Derudover kan overudnyttelse af grundvand fremskynde sulfatforurening.
Mangfoldigheden af sulfatkilder og deres effekter på det økologiske miljø tiltrækker i stigende grad forskeres opmærksomhed for at skelne kilderne og bestemme mekanismerne for svovl- og iltisotopvariationer i sulfat fra forskellige vandtyper samt de styrende faktorer.
Sporing af Sulfatkilder: Fra Traditionelt til Moderne
Den traditionelle metode til at spore sulfatkilder kombinerer studieområdets geologiske baggrund med hydrokemiske karakteristika. Denne metode er enkel, men dens nøjagtighed er ofte ringe. Med videnskabens og teknologiens fremskridt har forskere opdaget, at sulfat fra forskellige kilder har specifikke δ34S og δ18O værdier. Disse stabile isotoper fungerer som "fingeraftryk" og er blevet meget brugt til at identificere sulfatkilder og forstå de biogeokemiske cyklusser for svovl.
Stabile Isotoper: Svovl og Ilt
Svovl har fire naturlige stabile isotoper: 32S (95,02%), 33S (0,75%), 34S (4,21%) og 36S (0,02%). Svovlisotopsammensætningen karakteriseres normalt ved den relative forekomst af 32S og 34S. Ilt besidder tre stabile isotoper: 16O (99,759%), 17O (0,037%) og 18O (0,204%). Det traditionelle referencepunkt er Vienna Standard Mean Ocean Water (VSMOW). Svovlisotop-fraktioneringsmekanismen opdeles primært i ligevægtsisotop-fraktionering og kinetisk isotop-fraktionering. Den stabile isotopratio udtrykkes normalt som δ (delta) i promille (‰), hvilket er den stabile isotopratio i forhold til standarden. På grund af forskellige stoffers evne til at berige S og O eksisterer isotop-fraktionering ofte, når stoffets tilstand ændrer sig. Kinetisk isotop-fraktionering sker primært i ensrettede kemiske og biokemiske processer. Mikrobiel reduktion af sulfat under biokemiske processer vil resultere i større svovlisotop-fraktionering.
Forbehandlingsmetoder for Isotopanalyse
For at analysere svovl- og iltisotoper i sulfatprøver kræves specifikke forbehandlingsmetoder. Disse metoder sikrer, at sulfatet er i en form, der kan analyseres præcist af massespektrometri. Nogle af de anvendte metoder inkluderer grafitreduktionsmetoden, fluorineringsmetoden, højtemperatur-pyrolysemetoden, kemisk fældningsmetoden, triacidmetoden og flammeopvarmningsmetoden.
Grafitreduktionsmetoden: BaSO₄ reduceres med grafit ved 1100 °C for at producere CO₂ og CO. CO analyseres direkte eller omdannes til CO₂. Metoden er enkel, og resultaterne er nøjagtige med en præcision på ±0,2‰.
Fluorineringsmetoden: Sulfatet reageres med et stærkt oxidationsmiddel som fluor eller fluorhalogenid ved høj temperatur for at generere O₂. Den genererede O₂ omdannes til CO₂ i en grafitovn ved 700 °C. Analyseusikkerheden er omkring ±0,17‰. Denne metode kan også direkte måle iltisotopsammensætningen i O₂.
Højtemperatur-pyrolysemetoden: Prøverne pyrolytisk nedbrydes ved 1400 °C i nærvær af forniklet grafit for at producere CO. Metoden er enkel og bekvem og kan bruges til at bestemme δ18O-værdier i uorganiske og organiske prøver online. For sulfater kan δ18O analyseres med en standardafvigelse bedre end ±0,5‰.
Kemisk fældningsmetoden: Vandprøver filtreres og syres til pH ≤ 2 med HCl. Sulfatet fældes som BaSO₄ ved tilsætning af BaCl₂. Den opnåede barit renses og tørres. δ34S og δ18O i BaSO₄ bestemmes derefter. Analysepræcisionen for δ34S er bedre end ±0,2‰, og for δ18O ±0,5‰. Metoden med opløsning og genfældning (DDARP) kan fjerne nitrater og andre urenheder, hvilket gør bestemmelsen af iltisotop mere nøjagtig.
Triacidmetoden: En blandet opløsning af HCl, HI og H₃PO₂ bruges til at reagere med sulfatmineraler for at opnå Ag₂S, som oxideres til SO₂ for δ34S-bestemmelse. Kemisk proces er kompliceret og ubelejlig at betjene. Denne metode er primært egnet til sulfatmineraler.
Flammeopvarmningsmetoden: Sulfatmineralprøver halvsammensmeltes af Na₂CO₃-ZnO, og sulfatprøverne omdannes til BaSO₄. BaSO₄ og SiO₂ opvarmes derefter af flammen i vakuum for at generere SO₃, som reduceres af kobber til SO₂ for δ34S-bestemmelser. Metoden genererer skadelig gas og forbruger kvartsrør.
I øjeblikket er den forbehandlingsmetode, der almindeligvis anvendes til bestemmelse af sulfatisotoper, den kemiske fældningsmetode, som kombineres med elementaranalysator og stabilt isotop-massespektrometer, hvor svovl- og iltisotopværdierne af sulfat kan bestemmes.
Udviklingen inden for Isotopsporing
Forskningen i anvendelsen af stabile isotoper til identifikation af sulfatkilder har udviklet sig over mere end 40 år. I starten fokuserede man primært på hydrokemi eller anvendte kun δ34S-isotopen, hvilket ofte gav begrænset nøjagtighed på grund af overlap i værdierne fra forskellige kilder. Dette førte til udviklingen af metoder, der samtidig bestemmer både δ34S og δ18O. Eksempler på anvendelse af dobbelt-isotop tilgang inkluderer sporing af sulfat fra sulfider i Canada, fra atmosfærisk nedbør, sulfidoxidation og mineralopløsning i Kina, og fra evaporitære klipper i Portugal.
Med en dybere forståelse af processerne er forskere begyndt at generalisere modeller for bidragsrater fra forskellige sulfatkilder baseret på princippet om massebalance. Disse kvantitative modeller forsøger at estimere, hvor stor en procentdel af sulfatet der kommer fra hver potentiel kilde. En simpel model baseret på massebalance for svovl og ilt isotoper kan udtrykkes som:
δ34S = ∑ (fi × δ34Si)
δ18O = ∑ (fi × δ18Oi)
1 = ∑ fi
Hvor i repræsenterer de forskellige forureningskilder, δ34Si og δ18Oi er isotopværdierne for sulfat fra kilde i, og fi er bidragsraten (fraktion) fra kilde i. Denne type model giver et rammeværk for kvantitativ kildeallokering.
Udfordringer og Fremtidsperspektiver
Selvom sporingsteknologien for sulfatforurening i grundvand er udviklet, er nøjagtigheden stadig et område, der kræver forbedring. Tidligere studier var ofte kvalitative og baseret på enkelt-isotoper. Forskning bevæger sig nu mod dobbelte og multiple isotoper samt kvantitative metoder, men disse er endnu ikke fuldt modne. Desuden har mange studier fokuseret på overfladevand og regnvand, med relativt få studier om grundvandsforurening, især i områder med intensiv menneskelig aktivitet. Bestemmelse af de præcise "slut-medlem"-værdier (end-member values) for potentielle kilder er ofte baseret på litteraturdata frem for faktiske målinger i studieområdet, hvilket påvirker resultaternes nøjagtighed.
Fremtidig forskning bør derfor anvende multiple stabile isotopteknikker, såsom δD og δ18O for vand (H₂O) og 87Sr/86Sr for strontium, kombineret med hydrokemisk evolutionsteori og multivariate statistiske teknikker. Etablering af robuste kilde-fordelingsmodeller vil muliggøre kvantitative studier af forskellige kilders bidrag til sulfatforurening, hvilket kan give bedre grundlag for videnskabelig forebyggelse og kontrol.
Sporing af sulfatkilder i vandmiljøet er gået fra at bygge på hydrogeokemisk teori til i høj grad at anvende stabile isotopteknikker. Mens anvendelsen af δ34S og senere δ34S og δ18O har forbedret evnen til at identificere kilder, viser kompleksiteten af sulfatforureningskilder og isotop-fraktionering, at en enkeltstående tilgang sjældent er tilstrækkelig. For at sikre nøjagtig identifikation af sulfatkilder i vandmiljøet er det nødvendigt at udvikle multi-isotop sporingsteknologi, kombineret med hydrokemi, multivariate statistiske analysemetoder og kvantitative kilde-fordelingsmodeller.
Kunne du lide 'Kilder til Sulfat i Grundvand'? Så tag et kig på flere artikler i kategorien Læsning.